 A. Unsur dan Lambang Unsur
A. Unsur dan Lambang UnsurApabila dikaji, semua zat terbentuk dari bagian-bagian yang paling sederhana yang disebut unsur. Air dapat diuraikan lagi menjadi gas hidrogen dan gas oksigen.
Gula dapat diuraikan lagi menjadi karbon, oksigen, dan hidrogen. Dengan reaksi kimia biasa karbon, oksigen, dan hidrogen tidak dapat diuraikan lagi. Karbon, hidrogen, dan oksigen tergolong unsur. Unsur didefinisikan sebagai zat tunggal yang tidak dapat diuraikan lagi menjadi zat-zat lain yang lebih sederhana dengan reaksi kimia biasa.
Pada kondisi normal, banyak di antara unsur ini berupa benda padat, seperti tembaga, emas, besi, dan timbal. Merkuri atau yang lebih dikenal dengan nama air raksa dan brom merupakan contoh unsur yang berwujud cair. Oksigen dan nitrogen adalah contoh unsur yang berupa gas.
Sebenarnya bumi yang kita pijak ini terdiri dari berbagai macam unsur. Berikut ini delapan jenis unsur yang membentuk hampir 99% bagian kerak bumi.
Tabel unsur-unsur yang membentuk kulit bumi.
| Unsur | Persentase (%) |
| Aluminium Besi Kalium (potasium) Kalsium Magnesium Natrium Oksigen Silikon Unsur-unsur lainnya |
8,1 5,0 2,6 3,6 2,1 2,9 46,6 27,7 1,4 |
Unsur-unsur yang sudah dikenal ada yang berupa logam, bukan logam (nonlogam), dan semilogam. Logam adalah unsur yang memiliki sifat mengkilap dan umumnya merupakan penghantar listrik dan penghantar panas yang baik. Unsur-unsur logam umumnya berwujud padat pada suhu dan tekanan normal, kecuali raksa yang berwujud cair. Pada umumnya unsur logam dapat ditempa sehingga dapat dibentuk menjadi bendabenda lainnya. Beberapa unsur logam di antaranya besi,
emas, perak, platina, dan tembaga. Contoh unsur-unsur logam ditunjukkan pada tabel berikut.
Tabel unsur-unsur logam.
Adapun unsur nonlogam adalah unsur yang tidak memiliki sifat seperti logam. Pada umumnya, unsur-unsur nonlogam berwujud gas dan padat pada suhu dan tekanan normal. Contoh unsur nonlogam yang berwujud gas adalah oksigen, nitrogen, dan helium. Contoh unsur nonlogam yang berwujud padat adalah belerang, karbon, fosfor, dan iodin. Zat padat nonlogam biasanya keras dan getas. Unsur nonlogam yang berwujud cair adalah bromin. Perhatikan contoh unsur nonlogam pada tabel berikut.
Tabel unsur-unsur nonlogam.Selain unsur logam dan nonlogam ada juga unsur semilogam atau yang dikenal dengan nama metaloid. Metaloid adalah unsur yang memiliki sifat logam dan nonlogam. Contoh unsur-unsur jenis ini dapat kamu lihat padatabel berikut.
Tabel unsur-unsur semilogam.
Unsur semilogam ini biasanya bersifat semikonduktor. Bahan yang bersifat semikonduktor tidak dapat menghantarkan listrik dengan baik pada suhu yang rendah, tetapi sifat hantaran listriknya menjadi lebih baik ketika suhunya lebih tinggi.
Unsur memiliki nama dan lambang unsur agar lebih mempermudah cara penulisan dan mengenalnya. Adapun lambang unsur yang pernah dibuat adalah sebagai berikut.
1. Pendapat Para Ahli Kimia pada Abad Pertengahan
Lambang unsur berupa lambang dari macam-macam alat atau benda seperti pada gambar di bawah, ternyata lambang tersebut sulit dimengerti orang. Perhatikan gambar.

2. Pendapat John Dalton (1766—1844)
Lambang unsur yaitu berupa lingkaran seperti pada gambar di bawah ini. Lambang-lambang unsur menurut Dalton ini kurang praktis apabila digunakan untuk menuliskan zat yang majemuk.

3. Pendapat Jons Jacob Berzelius
Lambang unsur yang sekarang digunakan adalah seperti yang diusulkan oleh Jons Jacob Berzelius pada tahun 1813. Cara penulisan unsur tersebut dengan ketentuan diambil huruf pertama dari nama unsur dan ditulis dengan huruf kapital. Apabila ada dua unsur yang huruf depannya sama, maka unsur yang lain tadi selain memakai huruf pertama yang ditulis dengan huruf kapital diikuti salah satu huruf kecil yang terdapat dalam nama unsurnya.
Contoh:
Unsur Carbon dilambangkan C
Unsur Calsium dilambangkan Ca
Unsur Clorin dilambangkan Cl
Unsur Cobalt dilambangkan Co
Unsur Nitrogen dilambangkan N
Unsur Natrium dilambangkan Na
Unsur Neon dilambangkan Ne
Beberapa jenis unsur beserta lambangnya menurut Berzelius disajikan pada tabel berikut
Tabel Lambang Beberapa Unsur Logam, Nonlogam, dan Unsur Buatan Menurut Berzelius

Di alam semesta ini terdapat 114 unsur baik alami maupun buatan. Unsur alami terdiri atas 91 jenis unsur dan 23 unsur sisanya merupakan unsur buatan.
Unsur-unsur tersebut dikelompokkan berdasarkan kemiripan sifatnya. Pengelompokan unsur ini dinamakan Tabel Periodik Unsur. Perhatikan Tabel Periodik Unsur pada gambar brikut.

B. Senyawa
Senyawa adalah zat-zat yang tersusun atas dua unsur atau lebih yang bergabung secara kimia dengan perbandingan massa tertentu.
Air dan garam dapur merupakan salah satu contoh senyawa. Air dan garam dapur dikatakan senyawa karena tersusun atas dua unsur atau lebih. Air tersusun atas dua jenis unsur, yaitu hidrogen dan oksigen dengan perbandingan massa tertentu dan tetap. Garam dapur juga tersusun atas dua jenis unsur, yaitu natrium dan klorin dengan perbandingan massa tertentu dan tetap. Contoh lainnya, nitrogen dan hidrogen bergabung membentuk amoniak.
Sama halnya dengan unsur kimia, senyawa kimia diberi nama dan lambang agar memudahkan untuk dipelajari.
C. Rumus Kimia
Rumus kimia menunjukkan satu molekul dari suatu unsur atau suatu senyawa. Rumus kimia juga disebut rumus molekul. Rumus kimia digolongkan sebagai berikut.
1. Rumus Kimia Suatu Unsur
Dalam rumus kimia suatu unsur tercantum lambang atom unsur itu, yang diikuti satu angka. Lambang unsur menyatakan nama atom unsurnya dan angka yang ditulis agak ke bawah menyatakan jumlah atom yang terdapat dalam satu molekul unsur tersebut.
Contoh:
a. O2 berarti 1 molekul, gas oksigen.
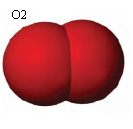
Dalam 1 molekul gas oksigen terdapat 2 atom oksigen
b. P4 berarti 1 molekul fosfor.
Dalam 1 molekul fosfor terdapat 4 atom fosfor.
Berbeda halnya dengan 2 O dan 4 P.
a. 2 O berarti 2 atom oksigen yang terpisah dan tidak terikat secara kimia.
b. 4 P berarti 4 atom fosfor yang terpisah dan tidak terikat secara kimia
2. Rumus Kimia Suatu Senyawa
Pada rumus kimia suatu senyawa tercantum lambang atom unsurunsur yang membentuk senyawa itu, dan tiap lambang unsur diikuti oleh suatu angka yang menunjukkan jumlah atom unsur tersebut di dalam satu molekul senyawa.
Contoh:
a. H2O berarti 1 molekul air
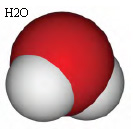
Dalam 1 molekul air terdapat 2 atom hidrogen dan 1 atom oksigen.
b. CO2 berarti 1 molekul gas karbon dioksida
Dalam 1 molekul gas karbondioksida terdapat 1 atom karbon dan 2 atom oksigen.
c. C12H22O11 berarti 1 molekul gula
Dalam 1 molekul gula terdapat 12 atom karbon, 22 atom hidrogen, dan 11 atom oksigen.
Jumlah senyawa yang ada di dunia ini sangatlah banyak. Oleh karena itu diperlukan sistem penamaan agar memudahkan kita untuk mempelajarinya. Pada pembahasan ini, kita hanya akan mempelajari tata nama senyawa biner yaitu senyawa yang tersusun dari dua jenis unsur.
Senyawa biner dapat merupakan gabungan dari atom nonlogam dengan nonlogam atau atom logam dengan atom nonlogam. Perhatikan kembali tabel periodik di atas untuk mengetahui unsur -unsur yang termasuk logam atau nonlogam.
1. Senyawa Biner dari Sesama Nonlogam
Aturan penulisan senyawa biner dari sesama nonlogam adalah sebagai berikut.
a. Unsur nonlogam yang terdapat di sebelah kiri pada urutan berikut, dituliskan terlebih dahulu.
B – Si – C – S – As – P – N – H – S – I – Br – Cl – O – F
Sebagai contoh, rumus kimia karbon dioksida dituliskan CO2 bukan O2C atau rumus kimia air dituliskan sebagai H2O bukan OH2.
b. Nama senyawa biner dari dua jenis unsur nonlogam diambil dari rangkaian nama kedua jenis unsur tersebut dan diberi akhiran -ida pada nama unsur yang kedua.
Contoh
CO : karbon monoksida
CaO : kalsium oksida
c. Jika pasangan unsur yang bersenyawa membentuk lebih dari sejenis senyawa, nama unsur tersebut dibedakan dengan menyebut angka dalam bahasa latin, seperti yang ditunjukkan pada tabel berikut.
| Angka | Bahasa latin |
| 1 2 3 4 5 6 7 8 9 10 |
mono di tri tetra penta heksa hepta okta nona deka |
CO : karbon monoksida
CO2 : karbon dioksida
NO2 : nitrogen dioksida
N2O3 : dinitrogen trioksida
2. Senyawa Biner dari Logam dan Nonlogam
Aturan penulisan senyawa biner dari logam dan nonlogam adalah unsur logam ditulis terlebih dahulu.
Contoh:
Garam dapur terdiri atas unsur logam (natrium) dan unsur nonlogam (klorin). Oleh karena itu rumus kimia garam dapur dituliskan NaCl (natrium klorida).
Rumus kimia dibedakan menjadi dua, yaitu rumus empiris dan rumus molekul. Rumus empiris adalah perbandingan paling sederhana dari atomatom yang membentuk senyawa. Contoh rumus empiris amoniak adalah NH3. Rumus kimia sesungguhnya dapat sama dengan rumus empiris atau kelipatan dari rumus empirisnya. Rumus sesungguhnya amoniak sama dengan rumus empirisnya, yaitu NH3. Rumus sesungguhnya dari asetilena adalah C2H2, yang merupakan kelipatan dua dari rumus empirisnya, yaitu CH.
Untuk senyawa molekuler, penting untuk diketahui berapa jumlah atom yang terdapat dalam setiap molekulnya. Jadi, rumus molekul dapat didefinisikan sebagai rumus kimia yang menyatakan perbandingan jumlah atom sesungguhnya dari atom-atom yang menyusun suatu molekul.
Dengan demikian, rumus empiris dan rumus molekul memiliki kesamaan dalam hal jenis unsurnya. Perbedaannya terletak pada perbandingan relatif jumlah unsur yang menyusun senyawa itu. Hubungan antara rumus empiris dan rumus molekul dari beberapa senyawa dapat kamu amati melalui tabel berikut.
Table hubungan antara rumus empiris dan rumus molekul beberapa senyawa.
| Rumus Senyawa |
Rumus Molekul |
Rumus Empiris |
| Air Butana Etana Etena Etuna Glukosa |
H2O C4H10 C2H6 C2H4 C2H2 C6H12O6 |
H2O (C2H5)n n = 2 (CH3)n n = 2 (CH2)n n = 2 (CH)n n = 2 (CH2O)n n = 6 |
1. Sifat Unsur
Sampai saat ini telah dikenal tidak kurang dari 114 macam unsur yang terdiri dari 92 unsur alam dan 22 unsur buatan. Berdasarkan sifatnya, unsur dapat digolongkan menjadi unsur logam, unsur nonlogam, serta unsur metaloid. Contoh unsur logam di antaranya besi, seng, dan tembaga. Contoh unsur nonlogam di antaranya karbon, nitrogen, dan oksigen. Silikon dan germanium tergolong metaloid.
Tabel perbandingan sifat antara unsur logam dan nonlogam.
| Unsur Logam |
Unsur Nonlogam |
| 1. Berwujud padat, kecuali raksa. 2. Bersifat kuat dan dapat ditempa. 3. Dapat menghantarkan listrik dan panas (bersifat konduktor). |
1. Dapat berwujud padat, cair, dan gas. 2. Bersifat rapuh dan tidak dapat ditempa. 3. Tidak dapat menghantarkan listrik dan panas (isolator), kecuali grafit. |
Air merupakan contoh senyawa. Unsur-unsur pembentuk air adalah oksigen dan hidrogen. Jadi, air terdiri dari gas oksigen dan gas hidrogen yang bergabung melalui reaksi kimia. Air dengan rumus kimia H2O, memiliki sifat yang berbeda dengan unsur-unsur pembentuknya, yaitu H2 dan O2 yang berupa gas. Air dapat diuraikan menjadi unsur-unsur pembentuknya, sehingga disebut senyawa. Adapun hidrogen serta oksigen disebut unsur. Jadi, senyawa adalah zat yang terbentuk dari unsur-unsur dengan perbandingan tertentu dan tetap melalui reaksi kimia. Jadi, sifat senyawa tidak sama dengan sifat unsur pembentuknya. Senyawa dapat dipisahkan menjadi unsur-unsur atau menjadi senyawa yang lebih sederhana melalui reaksi kimia.
Di dalam tiap senyawa unsur-unsur penyusunnya mempunyai perbandingan massa yang tetap dan tertentu. Misalnya,
a. Air (H2O), perbandingan massa unsur-unsur penyusunnya yaitu Hidrogen : Oksigen adalah 1 : 8
b. Gula (C12 H22 O11), perbandingan massa unsur-unsur penyusunnya yaitu Karbon : Oksigen : Hidrogen adalah 72 : 88 : 11
c. Etanol (C2 H5OH), perbandingan massa unsur-unsur penyusunnya yaitu Karbon : Oksigen : Hidrogen adalah 12 : 8 : 3
Beberapa contoh senyawa yang ada dalam kehidupan sehari-hari tercantum dalam tabel berikut.
Tabel Beberapa Contoh Senyawa dalam Kehidupan Sehari-hari
| N0 | Senyawa | Rumus | Kegunaan |
| 1 | Natrium Klorida | NaCl | Garam dapur |
| 2 | Sukrosa | C12H22O11 | Pemanis Gula |
| 3 | Asam Kloroda | HCl | Pembersih lantai |
| 4 | Asam asetat | CH3COOH | Cuka makan |
| 5 | Asam sulfat | H2SO4 | Pengisi aki (accu) |
| 6 | Air | H2O | Pelarut, pembersih |
| 7 | Urea | CO(NH2)2 | Pupuk |
| 8 | Asam askorbat | C6H8O6 | Vitamin C |
| 9 | Aspirin | C9H8O4 | Obat sakit kepala |
| 10 | Soda kue | NaHCO3 | Membuat kue |
Suatu campuran dapat merupakan gabungan unsur dengan unsur, unsur dengan senyawa, atau senyawa dengan senyawa. Misalnya, stainless steel (baja tahan karat) terbuat dari campuran besi, krom, dan nikel. Komposisi unsur-unsur penyusun suatu campuran tidak tertentu, sehingga rumus kimia suatu campuran tidak dapat ditentukan. Pemisahan campuran dapat dilakukan secara fisika.
Tanah diklasifikasikan dalam campuran, yaitu campuran berbagai macam unsur dan senyawa. Sifat asli zat-zat pembentuk campuran masih tampak, sehingga komponen penyusun campuran tersebut dapat dikenali dan dapat dipisahkan lagi. Perbandingan zat-zat penyusunnya tidak tentu seperti pada senyawa.
Ada dua macam campuran, yaitu campuran homogen dan campuran heterogen.
a. Campuran Homogen
Amati dengan saksama segelas air sirup. Bila air sirup tersebut jernih dan bercampur merata, dapat digolongkan sebagai campuran homogen. Campuran homogen ini biasa disebut larutan. Pada larutan, tiap-tiap bagian mempunyai susunan yang sama. Jadi di dalam larutan sirup tersebut terdapat dua penyusun larutan, yakni air dan gula. Air disebut pelarut, sedangkan gula disebut zat terlarut. Contoh campuran homogen lainnya adalah minuman ringan (soft drink) dan larutan pembersih lantai.
b. Campuran Heterogen
Amati segelas air yang dicampur dengan pasir. Apabila zat-zat penyusunnya bercampur secara tidak merata dan campuran ini tiap-tiap bagian tidak sama susunannya maka disebut campuran heterogen (perhatikan Gambar 3.8). Contoh campuran heterogen yang lain adalah air kopi (bentuk cair) dan campuran tepung dengan
air (bentuk padat). Susunan zat dalam suatu campuran sering dinyatakan dengan kadar dari zat-zat pembentuk campuran itu. Kadar suatu zat dalam campuran dapat dinyatakan sebagai jumlah zat dalam campuran dibandingkan jumlah seluruh campuran. Jumlah zat dapat dinyatakan dalam dalam massa (g, kg) atau volume (ml, l).

Adapun perbandingan tersebut dinyatakan dalam persen (%).Kadar Zat = (Jumlah Zat/Jumlah Campuran) x 100%
Tabel Perbedaan Antara Senyawa dan Campuran
| Keadaan | Unsur | Senyawa | Campuran |
| Penyusunnya | Tersusun dari satu jenis atom saja. | a. disusun oleh unsur-unsur b. hanya dapat dipisahkan secara kimia |
a. disusun oleh zat b. mudah dipisahkan secara fisik |
| Sifatnya | sifat senyawa berbeda dengan unsur-unsur penyusunnya | sifat zat penyusunnya masih tampak | |
| Proses Pembentukan | Tidak dapat diuraikan menjadi zat yang lebih sederhana dengan reaksi kimia biasa. | Dapat diuraikan menjadi unsur-unsur penyusunnya dengan reaksi kimia biasa. |
Dapat dipisahkan menjadi zat-zat penyusunnya secara fisika. |
| Perbandingan | perbandingan unsur-unsur penyusunnya tetap dan tertentu | perbandingan massa zat penyusunnya tidak tentu |
Referensi :
1. https://fembrisma.wordpress.com/science-1/unsur-senyawa-dan-campuran-2/
2. http://kimiapedia.com/unsur-senyawa-dan-campuran/
3. https://rahmiola.wordpress.com/kelas-ix/unsur-senyawa-dan-campuran/
4. https://bisakimia.com/2012/11/17/apa-itu-unsur-senyawa-dan-campuran/
5. www.academia.edu/16083199/Unsur-senyawa-dan-campuran
Tidak ada komentar:
Posting Komentar
Catatan: Hanya anggota dari blog ini yang dapat mengirim komentar.