Apa itu zat gas? Zat gas adalah Zat gas ialah
suatu zat atau benda yang mempunyai volume dan bentuk yang selalu
berubah-ubah sesuai dengan tempat (wadahnya). Contohnya; balon, ban sepeda
dan ban motor, gelas kosong, botol kosong, dan lain sebagainya. Dan juga
Zat gas memiliki bentuk dan volume yang berubah-ubah,
karena molekul-molekul gas dapat bergerak bebas.
Tampilkan postingan dengan label @Kel-K01. Tampilkan semua postingan
Tampilkan postingan dengan label @Kel-K01. Tampilkan semua postingan
Senin, 24 Desember 2018
Wujud Gas
Oleh: @K01-Irvin, @K02-Erlangga, @K03-Syaiful, @Kel-K01
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Kamis, 06 Desember 2018
Teori Ikatan Valensi
Teori
ikatan valensi (Valence Bond Theory, VBT) dikembangkan dari teori mekanika
kuantum yang berguna untuk menerangkan proses pembentukan ikatan kovalen secara
lebih baik dibandingkan model rumus titik-elektron Lewis.
Dalam kimia, teori
ikatan valensi atau teori ikatan valens menjelaskan sifat ikatan kimia dalam
suatu molekul dari sudut valensi atom. Teori ini menyimpulkan suatu aturan
bahwa atom pusat dalam suatu molekul cenderung untuk membentuk ikatan elektron
ganda sesuai dengan batasan geometris seperti kurang lebih ditentukan oleh
aturan oktet.
Sejarah
Berdasarkan
teori Bohr, diketahui bahwa teori Lewis-Langmuir tentang ikatan kovalen gagal
menjawab pertanyaan mendasar mengenai alasan mengapa atom membentuk ikatan,
atau mengapa molekul lebih stabil jika ada minimal dua atom yang membentuknya.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Senin, 26 November 2018
Ikatan Kimia
Ketika dua atom atau ion “berpegangan” dengan sangat erat, dapat dikatan bahwa di antaranya terdapat suatu ikatan kimia. Dalam pembentukannya, yang berperan adalah elektron valensi, yaitu elektron yang berada pada kulit terluar. Untuk memudahkan penggambaran elektron valensi pada atom suatu unsur dan ikatan yang terbentuk dapat digunakan simbol Lewis (simbol titik-elektron Lewis).
Simbol Lewis dari suatu unsur terdiri dari
simbol unsur tersebut dan satu titik untuk setiap satu elektron valensi yang
dimilikinya. Sebagai contoh, perhatikan simbol Lewis untuk unsur-unsur berikut.
Atom unsur-unsur golongan gas mulia
(golongan 18) dengan 8 elektron valensi memiliki sifat sangat stabil (tidak
reaktif), energi ionisasi tinggi, dan afinitas elektron rendah. Pada umumnya
semua atom berusaha untuk menerima, atau melepas, ataupun saling berbagi
elektron agar memiliki jumlah elektron yang sama dengan atom gas mulia dengan
nomor atom yang terdekat. Hal ini serupa dengan kehidupan manusia, di mana pada
umumnya manusia berusaha untuk mencapai kesejahteraan sebagaimana golongan gas
mulia. Hasil observasi ini mengacu pada rumusan teori: aturan oktet, yang
menyatakan bahwa atom-atom cenderung akan menerima, atau melepas, ataupun
saling berbagi (sharing) elektron sehingga memiliki 8 elektron valensi.
Atom-atom cenderung ingin berikatan karena
dengan adanya ikatan, energi potensial antara partikel positif dan partikel
negatif — entah antar ion dengan muatan yang berlawanan ataupun antar inti
dengan elektron-elektron di antaranya — akan lebih rendah. Ikatan kimia dibagi
menjadi 3 jenis berdasarkan 3 cara kombinasi dari unsur logam dan unsur
nonlogam, yakni logam dengan non logam (ikatan ionik), non logam dengan non
logam (ikatan kovalen), dan logam dengan logam (ikatan logam).
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Rabu, 14 November 2018
PARTIKEL DASAR ATOM
Oleh : Muhammad Irvin r (K01-Irvin), Erlangga Maulana S (K02-Erlangga), Syaiful Nur Cahyo (K03-Syaiful)
STRUKTUR ELEKTRON ATOM POLIELEKTRON
Konfigurasi
elektron adalah penyebaran/penyusunan elektron dalam kulit-kulit atom, jumlah
elektron maksimum yang menempati setiap kulit di rumuskan 2n^2.
Kuantum
adalah bilangan yang digunakan untuk menyatakan kedudukan.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Senin, 15 Oktober 2018
Kesetimbangan Kimia
Oleh: @K01-Irvin, @K02-Erlangga, @K03-Syaiful, @Kel-K01
Kesetimbangan kimia adalah keadaan reaksi bolak-balik dimana laju reaksi reaktan dan produk sama dan konsentrasi keduanya tetap. Kesetimbangan kimia hanya terjadi pada reaksi bolak-balik dimana laju terbentuknya reaktan sama dengan laju terbentuknya produk. Reaksi akan terjadi terus menerus secara mikroskopis sehingga disebut kesetimbangan dinamis.
Kesetimbangan kimia adalah keadaan reaksi bolak-balik dimana laju reaksi reaktan dan produk sama dan konsentrasi keduanya tetap. Kesetimbangan kimia hanya terjadi pada reaksi bolak-balik dimana laju terbentuknya reaktan sama dengan laju terbentuknya produk. Reaksi akan terjadi terus menerus secara mikroskopis sehingga disebut kesetimbangan dinamis.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Senin, 08 Oktober 2018
Oleh: 1. Muhammad Irvin (@K01-Irvin)
2. Erlangga M.S. (@K02-Erlangga)
3. Syaiful Nur Cahyo (@K03-Syaiful)
2. Erlangga M.S. (@K02-Erlangga)
3. Syaiful Nur Cahyo (@K03-Syaiful)
Termodinamika
II
1.
Hukum II
Termodinamika
Hukum II Termodinamika memberikan
batasan-batasan terhadap perubahan energi yang mungkin terjadi dengan beberapa
perumusan.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Senin, 01 Oktober 2018
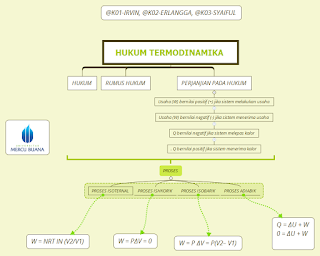
Termodinamika Hukum 1
Oleh: @K01-IRVIN, @K02-ERLANGGA, @K03-SYAIFUL, @KEL-K01
Pengertian
Termodinamika
Termodinamika merupakan ilmu yang mempelajari hubungan antara usaha dan kalor. Di dalam termodinamika kita mengenal adanya sistem dan lingkungan. Dalam termodinamika sistem diarttikan sebagai kumpulan dari benda – benda atau objek yang diteliti atau menjadi pusat perhatian kita sedangkan lingkungan diartikan sebagai benda atau objek yang berada di luar sistem.
Termodinamika merupakan ilmu yang mempelajari hubungan antara usaha dan kalor. Di dalam termodinamika kita mengenal adanya sistem dan lingkungan. Dalam termodinamika sistem diarttikan sebagai kumpulan dari benda – benda atau objek yang diteliti atau menjadi pusat perhatian kita sedangkan lingkungan diartikan sebagai benda atau objek yang berada di luar sistem.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Senin, 24 September 2018
Materi Stoikiometri
Oleh : @Kel-K01, @K01-Irvin , @K02-Erlangga, @K03-Syaiful.
Stoikiometri
: Konsep Mol.
1.
MASSA MOLAR
Pengertian massa molar
Massa molar
adalah massa zat yang sama dengan massa atom atau massa rumus zat tersebut
dinyatakan dalam gram. Massa molar ini sama dengan massa yang dimiliki oleh 1
mol zat yang
besarnya sama dengan massa atom relatif (Ar) atau massa molekul
relatif (Mr).
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Minggu, 16 September 2018
Atom & Teori Atom
oleh: M. Irvin (@K01-Irvin), Erlangga M.S. (@K02-Erlangga). Syaiful N.C. (@K03-Syaiful). @Kel-K01.
ATOM DAN TEORI ATOM
ATOM DAN TEORI ATOM
A. Atom
Atom merupakan bagian terkecil
dari suatu materi. meskipun ukurannya yang sangat kecil, Atom adalah partikel
paling kecil yang masih mempunyai sifat unsur.
Label:
@K01-Irvin,
@K02-Erlangga,
@K03-Syaiful,
@Kel-K01
Langganan:
Komentar (Atom)