Abstrak
Hukum termodinamika II yaitu tidak mungkin membuat
sebuah mesin kalor yang bekerja di suatu siklus semata-mata mengubah energi
panas yang diperoleh dari suatu reservoir pada suhu tertentu seluruhnya pada
usaha mekanik. Hukum kedua termodinamika mengatakan bahwa aliran kalor memiliki
arah; dengan kata lain, tidak semua proses di alam semesta adalah reversible (dapat
dibalikkan arahnya).
Hukum II Termodinamika
Hukum II Termodinamika
memberikan batasan-batasan terhadap perubahan energi yang mungkin terjadi
dengan beberapa perumusan.
- Tidak mungkin membuat mesin yang bekerja dalam satu siklus, menerima kalor dari sebuah reservoir dan mengubah seluruhnya menjadi energi atau usaha luas (Kelvin Planck).
- Tidak mungkin membuat mesin yang bekerja dalam suatu siklus mengambil kalor dari sebuah reservoir rendah dan memberikan pada reservoir bersuhu tinggi tanpa memerlukan usaha dari luar (Clausius).
- Pada proses reversibel, total entropi semesta tidak berubah dan akan bertambah ketika terjadi proses irreversibel (Clausius).
Bunyi Hukum II Termodinamika
Untuk menjelaskan tidak adanya reversibilitas para ilmuwan merumuskan prinsip baru, yaitu Hukum II Termodinamika, dengan pernyataan : “kalor mengalir secara alami dari benda yang panas ke benda yang dingin, kalor tidak akan mengalir secara spontan dari benda dingin ke benda panas”.Pengertian Entropi
Termodinamika menyatakan bahwa proses alami cenderung bergerak menuju ke
keadaan ketidakteraturan yang lebih besar. Ukuran ketidakteraturan ini dikenal
dengan sistem entropi. Entropi merupakan besaran termodinamika yang menyerupai
perubahan setiap keadaan, dari keadaan awal hingga keadaan akhir sistem.
Semakin tinggi entropi suatu sistem menunjukkan sistem semakin tidak teratur.
Entropi sama seperti halnya tekanan dan temperatur, yang merupakan salah satu
sifat dari sifat fisis yang dapat diukur dari sebuah sistem. Apabila sejumlah
kalor Q diberikan pada suatu sistem dengan proses reversibel pada suhu konstan,
maka besarnya perubahan entropi sistem adalah :
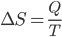
dengan:
ΔS = perubahan entropi ( J/K)
Q = kalor ( J)
T = suhu (K)
Mesin Pendingin
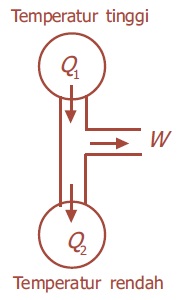
Mesin pendingin merupakan peralatan yang prinsip kerjanya berkebalikan dengan mesin kalor. Pada mesin pendingin terjadi aliran kalor dari reservoir bersuhu rendah ke reservoir bersuhu tinggi dengan melakukan usaha pada sistem. Contohnya, pada lemari es (kulkas) dan pendingin ruangan (AC). Bagan mesin pendingin dapat dilihat pada gambar berikut.Bagan proses penyerapan kalor pada mesin pendingin
 | ||
| https://physicsranggaagung.files.wordpress.com/2017/06/hukum-ii-termodinamika.jpg |
Ukuran kinerja mesin pendingin yang dinyatakan dengan koefisien daya guna merupakan hasil bagi kalor yang dipindahkan dari reservoir bersuhu rendah Q2 terhadap usaha yang dibutuhkan W.
dengan:
Kp = koefisien daya guna
W = usaha yang diperlukan ( J)
Q1 = kalor yang diberikan pada reservoir suhu tinggi ( J)
Q2 = kalor yang diserap pada reservoir suhu rendah ( J)
T1 = suhu pada reservoir bersuhu tinggi (K)
T2 = suhu pada reservoir bersuhu rendah (K)
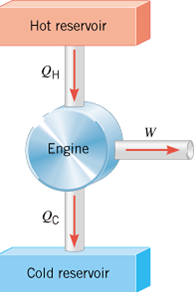
Penerapan hukum II termodinamika dapat diamati pada proses mengalirnya kalor pada mesin pemanas seperti ditunjukan pada gambar berikut.
 | |
| https://physicsranggaagung.files.wordpress.com/2017/06/picture1.png |
Bagan penerapan hukum II termodinamika pada mesin pemanas
Contoh Soal
- 1,5 m3 gas helium yang bersuhu 27oC dipanaskan secara isobarik sampai 87oC. Jika tekanan gas helium 2 x 105 N/m2 , gas helium melakukan usaha luar sebesar….
A. 60 kJ
B. 120 kJ
C. 280 kJ
D. 480 kJ
E. 660 kJ
Data :
V1 = 1,5 m3
T1 = 27oC = 300 K
T2 = 87oC = 360 K
P = 2 x 105 N/m2
W = PΔVV1 = 1,5 m3
T1 = 27oC = 300 K
T2 = 87oC = 360 K
P = 2 x 105 N/m2
Mencari V2 :
V2/T2 = V1/T1
V2 = ( V1/T1 ) x T2 = ( 1,5/300 ) x 360 = 1,8 m3
W = PΔV = 2 x 105(1,8 − 1,5) = 0,6 x 105 = 60 x 103 = 60 kJ (A)
Daftar Pustaka
Anonim, 2014, Hukum II Termodinamika
Ade, Firdaus Reza,
2018, Pengertian
Oktekkimiac, 2017,
Pengertian Etropi
@K17-Natalia @K19-Luthfiah @Kel-K06
BalasHapusSebuah mesin pendingin memiliki kalor pendingin sebanyak 3660 J dan membutuhkan kerja sebesar 3929 J. Berapakah efisiensi oleh mesin itu?
K=Qc/W
HapusK=3160J/3792J
K=83,3%